Специально разработанные атравматичные криозонды криотерапевтической системы ProSenseTM позволяют прицельно доставлять используемый хладагент (жидкий азот) в опухолевый очаг и охлаждать ткани до экстремально низких температур, разрушающий раковые клетки. Криозонды имеют закрытый контур и вакуумную изоляцию рабочей части, поэтому в процессе абляции жидкий азот не распространяется в ткани, а его газообразная форма после кипения на кончике криозонда возвращается обратно в систему. Газообразная форма жидкого азота в дальнейшем используется для проведения процедуры активного оттаивания для быстрого извлечения инструмента из ткани. Таким образом, выполняется прицельная криоабляция уничтожающая раковые клетки исключительно в зоне воздействия без повреждения смежных здоровых жизненно важных органов, структур и тканей. Программное обеспечение криотерапевтической системы ProSenseTM полностью контролирует процесс подачи жидкого азота в криозонды и предоставляет пользователю возможность проводить процедуры криоабляции как в ручном, так и в заранее запрограммированном, в зависимости от размеров и форм опухоли, автоматическом режиме.

Криозонды криотерапевтической системы ProSenseTM– прицельное воздействие без риска повреждения смежных здоровых органов, структур и тканей.
О криоабляции
Криоабляция («криотерапия», «криодеструкция») – это гипотермический локальный метод лечения, основанный на воздействии экстремально низких температур на патологические ткани и структуры. Впервые в медицинской практике отрицательные температуры были использованы в далеких 1845 и 1851 годах, однако, наиболее широко метод криоабляции начал использоваться в конце 90-х годов прошлого века с появлением новой аппаратуры, позволяющей безопасно и прицельно доставлять хладагент в зону интереса чрескожным доступом.
 |
|
|
Образование внеклеточного льда: дегидратация, денатурация белка, перекисное окисление липидов и увеличение свободных радикалов |
|
 |
 |
|
Формирование внутриклеточного льда: повреждение клеточной мембраны |
|
Криоабляция имеет несколько механизмов разрушающего действия тканей, принципиально отличающихся в центральной и транзиторной зонах криовоздействия. В центральной зоне воздействия возникает прямое и ишемическое повреждение клеток, а также иммуномодуляция. Прямое повреждение клеток в центральной зоне в основном происходит за счет клеточной дегидратации, которая неизбежно развивается при охлаждении тканей до температуры -20оС и ниже. Это обусловлено тем, что жидкость, находящаяся во внеклеточном пространстве, замерзает быстрее, чем жидкость, находящаяся внутри клеток, охлаждению которой препятствует клеточная мембрана. Поэтому возникает повышение осмолярности внеклеточной жидкости, которая под действием нарастающего осмотического градиента начинает вытягивать жидкость, находящуюся внутри клетки. Возникает клеточная дегидратация, которая сопровождается сморщиванием клеточной мембраны и повреждением клеточных органелл. Кроме того, значительно повышается концентрация ионов, нарушающих функцию целого ряда белковых структур. Дополнительным фактором разрушающего действия клеточных органелл является кристаллизация внутриклеточной жидкости. Стоит отметить, что необратимое повреждение клеток возникает исключительно в процессе оттаивания замороженной ткани в связи с устремлением внутрь клетки жидкости, находящейся во внеклеточном пространстве. Это связано с тем, что оттаивание жидкости внутри клетки происходит несколько медленней, а ее осмолярность значительно выше, чем жидкости во внеклеточном пространстве. Все эти процессы неизбежно приводят к разбуханию клетки с последующим разрывом ее мембраны. Ишемическое повреждение клеток в центральной зоне происходит вследствие разрушения эндотелия циркуляторного русла, сопровождающегося агрегацией тромбоцитов, сосудистым стазом, микротромбозом и холодовой вазоконстрикцией. Холодовое воздействие на ткани экстремально низких температур вызывает в организме значительно большую воспалительную реакцию, чем любое гипертермическое воздействие, в частности, чем радиочастотная абляция, поэтому криоабляция обладает значительной большей иммуногенностью. Это связано с тем, что гипотермическая криоабляция не полностью повреждает интрацитоплазматические органеллы и ультраструктурные компоненты клеток, делая их доступными и видимыми для иммунной системы организма. Клетки, подвергнутые прямому воздействию в центральной зоне, в результате их лизиса возникает выделение во внеклеточное пространство большого количества фрагментов ДНК, РНК, HSPsи HMGB1, приводящее к активации врожденного иммунитета, макрофагов и дендритных клеток. В транзиторной зоне под действием сублетальных температур гибель клеток происходит преимущественно путем апоптоза.
Прямое и непрямое повреждение раковых клеток и их внутриклеточных структур в процессе криоабляции зависит от многих факторов, таких как скорость заморозки, длительность холодового воздействия, температура замораживания, скорости оттаивания и числа проведенных циклов – заморозки-оттаивания. По этим причинам, одним из главных критериев эффективности криоабляции является медленное (пассивное) оттаивание замороженной области с проведением повторного цикла быстрой заморозки.
Область применения криоабляции
Эффективность криоабляция клинически доказана при лечении доброкачественных и злокачественных опухолей молочных желез, легких, печени, почек, костей и мягких тканей, предстательной железы и других органов.
-
Молочные железы:фиброаденома молочной железы, унифокальный рак молочной железы
-
Легкие:немелкоклеточный рак легкого, метастатический рак легкого
-
Печень:гепатоцеллюлярный рак печени, холангиоцеллюлярный рак печени, метастатический колоректальный рак печени, метастатический рак печени опухолей других локализаций
-
Почки:ангиомиолипома, почечноклеточный рак почки
-
Кости и мягкие ткани:первичный рак костей и мягких тканей, метастатический рак костей и мягких тканей, десмоидная опухоль мягких тканей, остеобластома кости, остеоидная остеома кости
-
Предстательная железа:локализованный рак предстательной железы, рецидивирующий рак предстательной железы
Преимущества криоабляции
В настоящее время криоабляция выполняется преимущественно чрескожным доступом, как менее травматичным по сравнению с лапароскопическим или открытым, с использованием различных систем лучевой визуализации тканей. Чрескожная гипотермическая криоабляция обладает уникальными преимуществами перед другими технологиями локального воздействия на ткани, такими как радиочастотная абляция, интерстициальная лазерная абляция, микроволновая абляция, интерстициальная ультразвуковая абляция и необратимая электропорация. К основным преимуществам чрескожного криовоздействия относятся:
-
Превосходная визуализация процесса абляции в режиме реального времени. Формирующийся в ткани ледяной шар обладает высокой эхогенностью, поэтому зона деструкции отчетливо визуализируется как при помощи ультразвукового сканирования, так и при использовании компьютерной томографии (КТ). Данное преимущество позволяет, во-первых, адекватно оценить зону абляции (быть уверенным, что опухоль полностью подвержена воздействию летальных отрицательных температур), во-вторых, значительно снизить риск повреждения смежных жизненно важных органов, структур и тканей (например, нервных стволов).
 |
 |
|
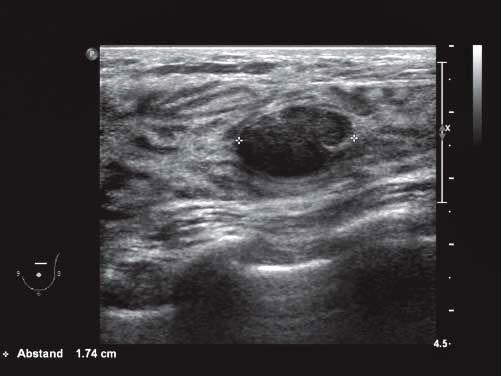
Ультразвуковое изображение фиброаденомы молочной железы до криовоздействия |
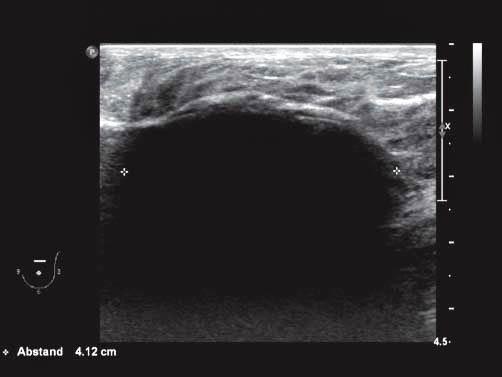
Ультразвуковое изображение фиброаденомы молочной железы в процессе криоабляции |
-
Безболезненность. Известно, что отрицательные температуры обладают анестезирующим действием, благодаря которому проведение криоабляции нет требует внутривенного наркоза. Процедуры, как правильно, в большинстве случаев проводятся под местной анестезией. Поэтому криоабляцию возможно выполнять онкологическим пациентам с противопоказаниями к общему наркозу и амбулаторным пациентам. Важно отменить, что болевой синдром после криоабляции значительно менее выражен, чем после гипертермических методов воздействия, поэтому процедуры криоабляции сопровождаются быстрым восстановлением и не требуют длительного пребывания в стационаре. К примеру, при криоабляции рака почки нередко пациентов выписывают из клиники в день или на следующий день после вмешательства.
-
Низкий риск повреждения жизненно важных органов. Криоабляция в значительно меньшей степени, чем гипертермические методы такие как лазерная, радиочастотная, микроволновая или ультразвуковая абляция, повреждает соединительно-тканные структуры (коллагеновые волокна) различных органов и тканей. По этим причинам криоабляция является более безопасным методом при проведении лечения опухолевых узлов, прилежащих к жизненно важным органам и структурам, например, желчному пузырю, толстому кишечнику, мочевому пузырю и другим органам.
-
Иммуногенность. Криоабляция, в отличие от других методов локального воздействия на ткани, в частности гипертермических, вызывает более выраженную воспалительную реакцию организма, вызванную выделением из поврежденных клеток большого числа опухолевых антигенов. Данное преимущество криоабляции позволяет в будущем комбинировать криовоздействие с различными методами иммунотерапии для стимуляции системного иммунного ответа организма (противоопухолевого иммунитета).